Este artículo fue actualizado por última vez el abril 6, 2024
Nuestro futuro con vacunas de ARNm: la panacea para todo lo que nos aqueja
Nuestro futuro con vacunas de ARNm: la panacea para todo lo que nos aqueja
Durante la pandemia, la tecnología de la vacuna de ARNm ocupó un lugar central en la batalla contra la vacuna contra el SARS-CoV-2, la primera vez que la tecnología se utilizó en algo que no fueran ensayos de laboratorio relativamente pequeños. A pesar de la creciente evidencia de que estas vacunas eran responsables de una cantidad y variedad significativa de efectos secundarios adversos y de que no eran muy efectivas para prevenir la propagación de COVID-19, esto parece haber abierto la puerta a un uso aún más amplio del ARNm. vacunas.
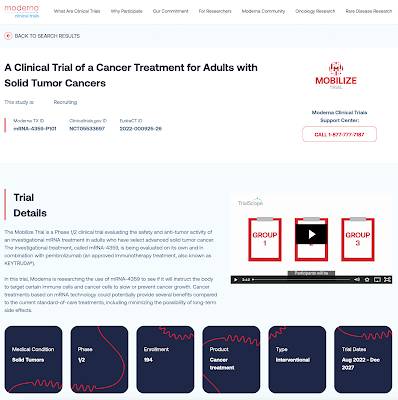
Aquí hay una captura de pantalla. del sitio web de ensayos clínicos de Moderna que recuerda que Moderna fue el proveedor de la vacuna de ARNm Spikevax COVID:
Este ensayo clínico de fase 1/2 evaluará la seguridad y eficacia de la vacuna mRNA-4359 de la compañía, que está diseñada para retardar o prevenir el crecimiento de cánceres de tumores sólidos en adultos. Aparentemente, las pruebas preclínicas en modelos de cáncer tanto celulares como animales proporcionaron evidencia inicial de que la vacuna mRNA-4359 tenía un impacto en el sistema inmunológico, lo que proporcionó la justificación necesaria para ofrecerla en los ensayos clínicos de fase 1/2.
Los participantes en el estudio deben:
1.) Tener 18 años de edad o más
2.) Tener cáncer localmente avanzado o metastásico confirmado: incluye: melanoma cutáneo, NSCLC, cáncer de vejiga no músculo invasivo, carcinoma de células escamosas de cabeza y cuello, MSS CRC, carcinoma de células basales o cáncer de mama triple negativo. También incluye: confirmado melanoma localmente avanzado o metastásico o NSCLC que hayan recibido terapia previa con inhibidores de puntos de control
3.) Haber experimentado progresión de la enfermedad después de recibir terapias de atención estándar o ser intolerante al tratamiento de atención estándar
Los participantes que tengan tumores o metástasis activos en el sistema nervioso central quedan excluidos del estudio.
Se espera que los participantes asistan a 17 visitas al sitio del ensayo durante tres años con un período de tratamiento de aproximadamente 6 meses seguido de un seguimiento de seguridad de 90 días y un período de seguimiento de dos años. La vacuna se administrará mediante inyección intramuscular y pembrolizumab se administrará por vía intravenosa. Me pareció interesante que este ensayo de Fase 1/2 esté tardando tres años en
completo (sin incluir otro ensayo de fase 3), mientras que los ensayos previos al lanzamiento de las vacunas de ARNm COVID-19 se llevaron a cabo en menos de un año.
Los participantes serán asignados a uno de los tres grupos de tratamiento de la siguiente manera:
1.) Brazo 1a
Este grupo tendrá como objetivo tratar a adultos con cáncer localmente avanzado o metastásico (melanoma cutáneo, carcinoma de pulmón de células no pequeñas [NSCLC], cáncer de vejiga no músculo invasivo, carcinoma de células escamosas de cabeza y cuello, cáncer colorrectal estable microsatélite [MSS CRC ], carcinoma de células basales o cáncer de mama triple negativo) que hayan recibido previamente tratamiento para su cáncer.
Los participantes asignados al Grupo 1a recibirán el tratamiento en investigación.
El objetivo del Grupo 1a es determinar una dosis segura del tratamiento en investigación.
2.) Brazo 1b
Este grupo incluirá adultos con melanoma localmente avanzado o metastásico o NSCLC que previamente recibieron inmunoterapia (llamada terapia con inhibidores de puntos de control) para su cáncer.
Los participantes asignados al Grupo 1b recibirán el tratamiento en investigación en combinación con pembrolizumab.
El objetivo del Grupo 1b es determinar una dosis segura del tratamiento en investigación en combinación con pembrolizumab.
3.) Grupo farmacodinámico
Además de los objetivos del Grupo 1b, los investigadores también evaluarán cómo el tratamiento en investigación y pembrolizumab afectan el sistema inmunológico y el cáncer en un grupo llamado Grupo Farmacodinámico (PD).
Los participantes inscritos en PD Arm recibirán el tratamiento en investigación y también se les pedirá que proporcionen muestras adicionales de sangre y tejido.
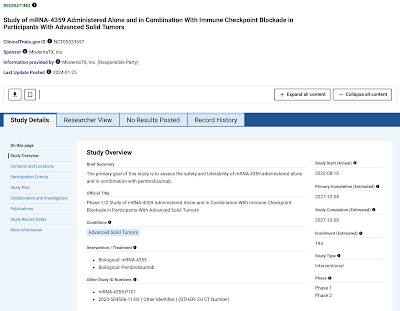
Aquí Esta es la descripción general del estudio del sitio web de ensayos clínicos del gobierno de EE. UU.:
El estudio es un ensayo no aleatorio, lo que significa que todos los pacientes reciben el mismo tratamiento. También es de etiqueta abierta, lo que significa que los médicos y los pacientes saben qué brazo de tratamiento están recibiendo, a diferencia de los ensayos ciegos en los que los pacientes no conocen su curso de tratamiento. También notarás que no existe un grupo de placebo.
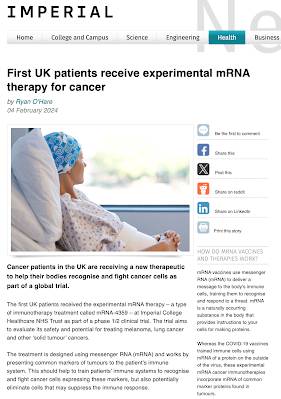
Imperial College en el Reino Unido, sede de Profesor Neil Ferguson, modelador de la pandemia de COVID-19, autor de un informe defectuoso que condujo directamente al bloqueo de la pandemia global, anunció recientemente la siguiente:
En el Reino Unido, la prueba se lleva a cabo en colaboración entre el Imperial College London y el Imperial College Healthcare NHS Trust. El primer paciente que recibió la vacuna mRNA-4359 fue inyectado a finales de octubre de 2023.
A finales de marzo de 2024, Moderno también anunció que estaba avanzando tres de sus vacunas de ARNm a ensayos clínicos de última etapa, incluidas vacunas para el citomegalovirus (CMV), el virus de Epstein-Barr (EBV), el virus del herpes simple (HSV) y el virus de la varicela-zoster (VZV) (es decir, el herpes zóster). Entre los ensayos de vacunas adicionales de ARNm encontramos las siguientes:
1.) CMV: CMVictory es un ensayo fundamental de fase 3 que evalúa el ARNm-1647 contra la infección primaria por CMV en mujer 16 a 40 años de edad. El ensayo es un estudio aleatorizado, ciego al observador y controlado con placebo diseñado para evaluar la eficacia, seguridad e inmunogenicidad del ARNm-1647. El ensayo está completamente inscrito con aproximadamente 7300 participantes de 290 sitios clínicos en todo el mundo.
2.) EBV: las vacunas candidatas contra el EBV de Moderna están diseñadas para abordar múltiples afecciones asociadas al EBV, incluida la prevención de la IM (mRNA-1189) y la EM y el trastorno linfoproliferativo postrasplante, una subcategoría de linfoma en pacientes con trasplante de órganos sólidos (mRNA-1195). ). El ensayo de fase 1 para mRNA-1189 fue diseñado para probar la seguridad, reactogenicidad e inmunogenicidad de cuatro niveles de dosis diferentes en participantes de 12 a 30 años de edad en los EE. UU. El estudio aleatorizado, ciego al observador y controlado con placebo mostró que mRNA-1189 fue inmunogénico y generalmente bien tolerado en todos los niveles de dosis. La compañía está avanzando el ARNm-1189 hacia un ensayo fundamental de fase 3.
El ensayo de fase 1 para mRNA-1195 fue diseñado para probar la seguridad, reactogenicidad e inmunogenicidad de dos medicamentos en cuatro niveles de dosis diferentes en participantes sanos seropositivos para EBV de 18 a 55 años de edad en los EE. UU. El estudio controlado está completamente inscrito.
3.) HSV: el primer ensayo de fase 1/2 en humanos con inscripción completa de ARNm-1608 está diseñado para probar la seguridad y la inmunogenicidad y establecer una prueba de concepto de beneficio clínico en adultos de 18 a 55 años de edad con enfermedad recurrente. Herpes genital HSV-2. El estudio controlado, aleatorizado, ciego al observador 1:1:1:1 está completamente inscrito con 300 participantes en los EE. UU.
4.) VZV: la vacuna candidata VZV mRNA-1468 de Moderna tiene datos iniciales disponibles de un ensayo de fase 1/2, que fue diseñado para probar la seguridad y la inmunogenicidad en adultos sanos de 50 años de edad o más en los EE. UU. La aleatorización 1:1: El estudio 1:1:1, ciego al observador y controlado con activo de mRNA-1468 provocó fuertes respuestas de células T específicas de antígeno un mes después de la segunda dosis y, en general, fue bien tolerado. Los resultados del primer análisis intermedio respaldan el desarrollo clínico adicional del ARNm-1468 para la prevención de la culebrilla. Los resultados adicionales del estudio de fase 1/2 en curso estarán disponibles a finales de este año, incluidos datos de persistencia. La compañía está planeando una prueba fundamental de fase 3.
Modern también está esperando aprobaciones regulatorias para mRNA-1345, la vacuna candidata contra el virus sincitial respiratorio (VRS) de la compañía que actualmente se encuentra en la fase 2/3 de un ensayo aleatorizado, ciego al observador, controlado con placebo y basado en casos.
Al observar las enfermedades humanas a través de la lente de Moderna, se puede ver que el experimento de la vacuna de ARNm en la humanidad continuará sin cesar. Moderna quiere hacernos creer que esta tecnología recientemente comercializada es la solución a cualquier cosa que nos aqueje y parece bastante capaz de ignorar la larga lista de posibles efectos adversos para la salud de esta tecnología que están observando los médicos y clínicos de todo el mundo. No obstante, se está avanzando a toda velocidad en lo que respecta a la tecnología de ARNm.
Vacuna de ARNm

Be the first to comment